اثر پوششي و بار مؤثر هسته
الكترونهايي كه در لايههاي خارجي یک اتم قرار دارند، هم بار مثبت ناشي از هسته و هم بار منفي الكترونهاي لايههاي دروني را احساس ميكنند. به علت وجود الكترونهاي لايههاي دروني و دافعهي آنها بار خالصي كه الكترونهاي لايههاي خارجيتر احساس ميكنند، كمتر از بار واقعي هسته است. به اصطلاح ميگوييم كه الكترونهاي دروني جاذبه يا بار هسته را از الكترونهاي خارجيتر پوشش (حايل) ميدهند و به اين اثر، اثر حائل يا اثرپوششي ميگويند. به بار مثبتی که یک الکترون از طرف هسته با در نظر گرفتن اثر پوششی الکترون های دیگر احساس می کند بار مؤثر هسته گفته می شود و با Z* یا Zeff نشان داده می شود. می توان گفت Z* همان بار هسته دیده شده توسط یک الکترون است، به شرطی که الکترونهای دیگر نباشند. شکل بعدی نمایشی برای این مطلب است:
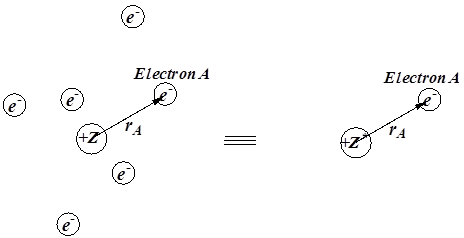
همانطور که شکل نیز نمایش می دهد، برای الکترون A فرقی نمی کند که در فاصله rA از یک هسته با بار مثبت برابر +Z در کنار حضور الکترونهای دیگر قرار گیرد یا از طرف دیگر در همان فاصله rA از یک هسته با بار مثبت برابر +Z* بدون حضور الکترونهای دیگر قرار گیرد.
در صورتیکه اثر پوششی الکترون های دیگر را با S نمایش دهیم، رابطه زیر را برای Z* خواهیم داشت:
Z*=Z-S = Zeff
برای یک الکترون در درجه ی اول اثر پوششی الکترون های زیرین و در درجه دوم اثر پوششی کمتر الکترون های هم لایه مهم است. برای یک الکترون از اثر پوششی الکترون های لایه خارجی می توان صرف نظر کرد. شکل بعدی را در نظر بگیرید.
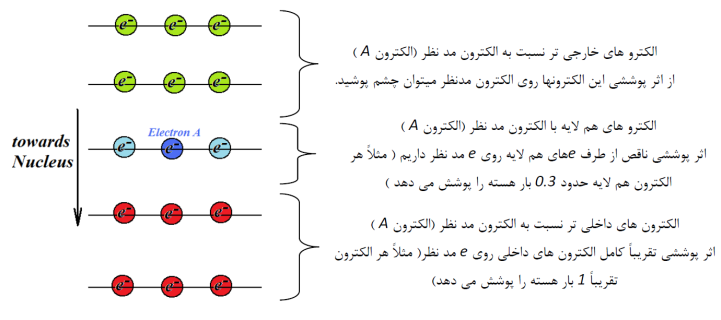
الكترونهاي داخلی تر اثر پوشش بيشتري روي الكترونهاي ديگر اعمال ميكنند و از طرفي اثر پوششي كمتري از طرف الكترونهاي ديگر ميبينند. بنابراين با كاهش n و نزديكتر شدن الكترونها به هسته، بار مؤثر هسته افزايش مييابد. نوع زيرلايه و شكل اوربيتال نيز در بار مؤثر هستهي احساس شده توسط الكترونها مؤثر است. با كاهش عدد کوانتومی فرعی بار مؤثر هستهي احساس شده افزايش مييابد.
مثال: بار موثر هسته 1s,2s,3s را با هم و 4s,4p,4d,4f را با هم مقایسه نمایید.
حل:
با توجه به مطالب یاد شده داریم:
![]()
*****
||||||||||||||||||||||||||||||||||||||||||||||||||
**************************************************
سایت: www.youngchemist.com
مولف: محمد شاهی
نظرات، پیشنهادات و انتقادات: chemistry.shahi@gmail.com
**************************************************
||||||||||||||||||||||||||||||||||||||||||||||||||